脱氧核糖核酸通常又称DNA,是染色体的主要组成部分。
脱氧核糖核酸携带合成RNA和蛋白质的遗传信息,并通过半保留复制指导生物发展和生活技能的操作。脱氧核糖核酸由脱氧核糖、磷酸盐和碱基组成,碱基包括腺嘌呤、鸟嘌呤和胸腺嘧啶等。DNA的结构为双螺旋结构,结合非常稳定。脱氧核糖核酸可以存储和传输遗传信息,细胞通过DNA复制遗传信息,并通过互补的含氮碱基序列传递遗传信息。
日常生活中,DNA可以用来识别罪犯和犯罪行为、指纹识别和亲子鉴定等,并且法医可以通过从血液、皮肤和唾液等组织和体液中分离出DNA进行法医鉴

图片来源:pixabay
大约40亿年前,地球上最伟大的演化正在悄无声息地进行着:一个大分子神奇地获得了自我复制的能力,由此演化出地球上最早的生命。这个神奇的大分子究竟是什么?此前的研究提出了包括DNA、RNA在内的一系列猜想。而最近,一项发表在《自然·通讯》的研究提出了全新的观点:答案可能不是DNA,也不是RNA,而是一类核酸类似物——XNA。
生命从何而来
就像工厂一样,我们的细胞内也存在着一条生产流水线。被称为脱氧核糖核酸(DNA)的分子,通过转录将遗传信息传递给核糖核酸(RNA),然后RNA通过翻译合成蛋白质。这套细胞内的流水线,我们称之为“中心法则”。
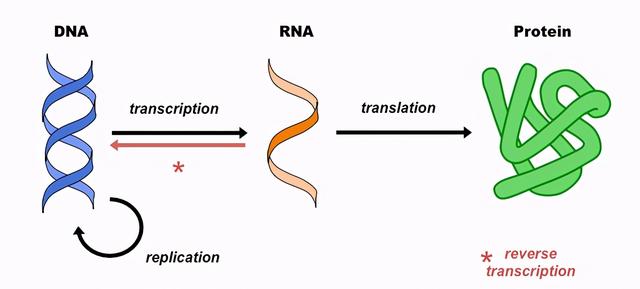
中心法则示意图。(图片来源:BioNinja)
自1957年提出以来,中心法则在科学家的努力下被不断完善。其中,对中心法则最重要的一条修改,源自逆转录酶的发现。1970年,两个独立的研究团队几乎同时发现了RNA肿瘤病毒中存在一种酶(蛋白质),这种酶能够以RNA作为模板,合成DNA。这个发现令人震惊,它不仅证明了RNA中的信息可以逆向流入DNA中,也向我们提出了一个“鸡生蛋”的问题:DNA和RNA,谁首先出现,谁才是生命的源头呢?
这个问题的答案似乎显而易见。如今地球上的生物在外形和生活环境上都迥然不同,但它们却有一个共同之处——将DNA作为遗传物质,一代代地生存、繁衍与演化。即使是已知的地球上的最早生命,35亿年前的蓝藻也凭借着DNA中携带的信息,进行光合作用,为地球上氧气的聚集创造了条件。DNA是生命之源,似乎毋庸置疑。
但这一假说存在一个致命缺陷。那就是DNA除了携带遗传信息之外,没有任何催化化学反应的功能。失去了蛋白质的辅助,DNA甚至无法进行复制,代代相传更是不可能。而蛋白质和DNA两种大分子聚合物在地球早期同时出现的概率,更是小得可怜。
“RNA世界”假说
作为DNA和蛋白质之间传递信息的桥梁,RNA引起了科学家的注意。早在1962年,美国生物学家亚历山大·里奇(Alexander Rich)就提出,RNA或许可以同时履行DNA和蛋白质的功能,即携带遗传信息和催化化学反应。但在当时,具有酶性质的RNA还尚未被发现。直到20年后,科学家在四膜虫中发现了可以实现自剪接的RNA分子,才证明了RNA可以催化化学反应。因此,RNA分子具备了作为生命起点的可能性。1986年,分子生物学家沃尔特·吉尔伯特(Walter Gilbert)将这一假说正式命名为“RNA世界”假说。
支持“RNA世界”假说的最有力的证据是核糖体的存在。核糖体是细胞中合成蛋白质的工厂,在几乎所有细胞中广泛存在。核糖体中合成蛋白质的活性位点由RNA组成,而蛋白质仅在RNA内核外起着结构支撑的作用。因此,许多科学家都将核糖体视作RNA世界的遗迹。或许正如弗朗西斯·克里克(Francis Crick)在1968年所预测的那样:“原始的核糖体可能完全由RNA组成。”
此外,也有其他研究为“RNA世界”假说提供佐证。例如,要支持生命,就需要RNA能够进行自我复制。今年3月,发表在《科学》杂志上的一项研究,向证明这一点迈出了重要一步。来自加拿大西蒙弗雷泽大学的研究团队通过实验室体外进化技术,筛选出一种RNA聚合酶。它能以一条RNA为模板,合成另一条RNA链,从而实现以RNA为遗传物质的复制和转录。研究人员表示,“我们的这项发现表明,在地球早期也可能存在相似的RNA酶,能够执行如此复杂的功能。”
然而,RNA酶也恰恰是“RNA世界”假说的缺陷之一。“如果有人接受了‘RNA世界’假说,他们将陷入另一个两难境地,”斯克利普斯研究所的生物学家拉迈克尔·罗伯逊(Michael Robertson)和杰拉尔德·乔伊斯(Gerald Joyce)指出,“如果没有演化的作用,能够催化RNA聚合反应的RNA酶不可能出现;但如果一开始没有RNA酶的话,也不存在生存优势,演化也无从谈起。”他们表示,一种可能的解释是,在地球早期RNA能够自发进行复制,不需要酶的作用;另一种可能则是,在RNA之前或许还存在其他遗传物质,“如果有研究者认为RNA不是最早的遗传物质,他不仅需要证明地球早期条件可以支持另一种信息载体的存在,还要证明这种信息载体可以在没有酶的条件下,进行自主复制。”
XNA世界
近日,发表在《自然·通讯》(Nature Communications)上的一篇研究,向解决罗伯逊和乔伊斯提出的问题迈出了重要一步。来自日本名古屋大学的生物工程学家,同时也是该研究的第一作者村山惠司(Keiji Murayama)表示,“在RNA世界前,可能还存在一个异核酸(xeno nucleic acid,XNA)世界。与RNA不同,XNA分子可能不需要酶催化就能够进行自主复制。”
村山提到的XNA是一类核酸类似物的统称。一般来讲,组成核酸的核苷酸包括了糖类、碱基和磷酸基团三部分。而DNA、RNA和XNA只在糖类组成上有所不同:DNA和RNA中的糖分子分别为脱氧核糖和核糖,而由其他糖组成的核酸类似物则统称为XNA。
关于XNA的最初设想,是将其用于制造合成生命。但随着科学家在实验室中制造出越来越多的XNA,他们注意到一些XNA不仅结构上比RNA更加简单,同时也能够进行复制,并且还能与RNA进行配对。因此有人提出了一个大胆的设想:XNA有可能先于RNA出现,是地球上最早的生命遗传物质。
莱斯利·奥格尔(Leslie Orgel)是一位研究生命起源的英国化学家,他曾表示:“我们很难理解组成RNA的单体——β-核苷酸,在地球早期环境中是如何形成的。因此许多讨论都强调了寻找比RNA更简单的遗传信息载体的重要性。这里的‘简单’不是指结构上更简单,而是指在地球早期环境中更容易合成。”
这促使科学家开始寻找其他合成简单,并且能够携带遗传信息的核酸类似物。此次最新研究的主角就是其中的一种。这种名为非环形L-苏氨醇核酸(L-aTNA)的XNA分子能够与自身以及DNA、RNA形成稳定的双螺旋结构。由于L-aTNA是非环状结构,因此相较于含有环状结构的RNA来说更容易合成。
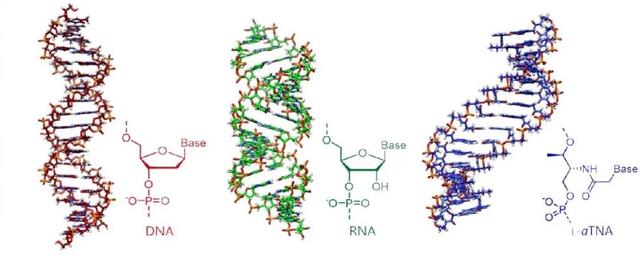
DNA、RNA与L-aTNA的结构示意图(图片来源:村山惠司)
正如罗伯逊和乔伊斯所指出的,要证明L-aTNA有可能先于RNA出现,需要证明它可以在没有酶的条件下进行自主复制。这意味着,需要利用化学反应在两个L-aTNA单体分子之间形成磷酯键,从而将两个分子连接起来。此前研究表明,一种叫做N-氰基咪唑(N-cyanoimidazole,CNIm)的缩合剂能够促使磷酸基团和邻近的羟基形成磷酯键。之前也有研究利用N-氰基咪唑成功地合成了不同的DNA分子结构。村山和同事认为,考虑到L-aTNA与DNA在结构上的相似性,N-氰基咪唑应该也能够介导L-aTNA间磷酯键的形成。
为了验证这个猜想,研究人员将两条L-aTNA短链与一条序列互补的L-aTNA长链混合在一起,并向其中加入了少量N-氰基咪唑,以及催化反应进行的二价锰离子,然后放置在4˚C下进行反应。结果发现,两条L-aTNA短链能够以长链为模板互相连接,在4小时内,连接效率达到了95%。
但DNA和RNA的复制,并不只是两条短链的简单连接,而是需要以长链为模板,连续连接多条短链。最终,利用碱基互补原理,形成一条长链。为了探究L-aTNA是否能在无酶条件下实现这一点,研究人员首先合成了2~5个核苷酸长度的序列随机的L-aTNA片段,然后将这些片段与引物、模板链混合,最终在2个小时内成功合成了16个核苷酸长度的L-aTNA,转换效率达到90%。村山表示:“据我们所知,这是首次在无酶条件下,让随机的非环状XNA片段之间形成磷酯键,并按照模板进行延伸。”
如果L-aTNA的确是比RNA更古老的遗传物质,那么基于L-aTNA的原始生物,是如何转变为以RNA为遗传物质的?最新研究表明,这可能与混合核酸分子的形成有关。村山及其同事发现L-aTNA能够以DNA和RNA作为模板进行延伸。“我们的数据显示,L-aTNA可能先于RNA出现。因为在N-氰基咪唑存在时,L-aTNA可以将现存的两种核酸作为模板;反之,DNA也可以将L-aTNA作为模板进行延伸,”研究报告进一步指出,“这表明L-aTNA与这两种核酸分子之间可以进行信息传递。”由于此项研究中使用的L-aTNA是在实验室中合成得到的,接下来研究团队准备进一步探究,L-aTNA是否能够在地球早期环境中合成。
事实上,关于地球上最早生命遗传物质的讨论,远不止于DNA、RNA和L-aTNA,还有更多你或许从未听说过的XNA分子,例如GNA、HNA、PNA。东京工业大学地球生命科学研究所的研究团队曾通过计算机模拟,生成了近150万种核酸类似物。论文的第一作者,地球生命研究所副教授吉姆·克利夫斯(Jim Cleaves)表示:“现代生物世界存在DNA和RNA两种核酸,或许还存在20~30个能结合核酸的核酸类似物。我们想知道是否还存在更多的类似物,但搜索出的数目之多,远超我们的想象。
对于我们来说,这些不同的核酸或许只是不同字母的排列组合。但事实上,它们中蕴含着地球早期生命的关键信息。透过它们,我们得以窥见一场最伟大的演化:约40亿年前的地球上,小分子物质如何成为大分子物质,而这些大分子又如何获得“智慧”,自我繁殖,创造出地球上第一个生命。
撰文:洪艺瑞 审校:吴非
原始论文:
Murayama K, Okita H, Kuriki T, et al. Nonenzymatic polymerase-like template-directed synthesis of acyclic l-threoninol nucleic acid[J]. Nature communications, 2021, 12(1): 1-9.
参考链接:
Cojocaru R, Unrau P J. Processive RNA polymerization and promoter recognition in an RNA World[J]. Science, 2021, 371(6535): 1225-1232.

